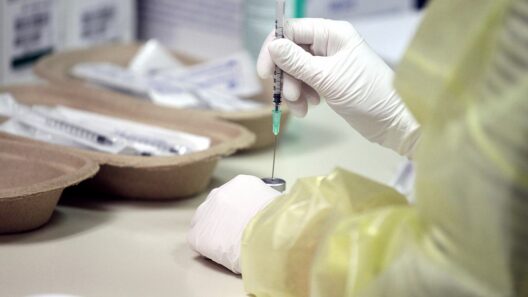
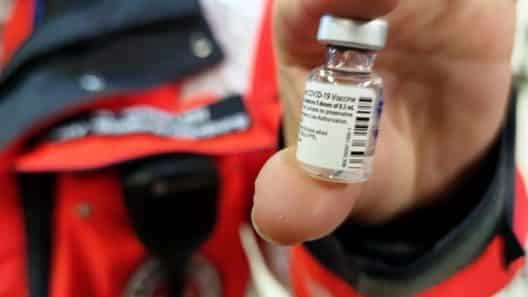
Amsterdam (dts Nachrichtenagentur) – Die Europäische Arzneimittel-Agentur (EMA) empfiehlt offiziell die Zulassung des proteinbasierten Corona-Impfstoffs von Novavax. Der Wirkstoff mit dem Handelsnamen Nuvaxovid könne bei Personen ab 18 Jahren eingesetzt werden, teilte die EU-Behörde am Montag mit.
Der Humanarzneimittelausschuss (CHMP) der EMA sei nach der Prüfung von Studienergebnissen einvernehmlich zu dem Schluss gekommen, dass die Daten zum Impfstoff robust seien und die EU-Kriterien für Wirksamkeit, Sicherheit und Qualität erfüllten. Zur Wirksamkeit von Nuvaxovid gegen die neue Omikron-Variante des Coronavirus liegen bisher allerdings nur begrenzte Daten vor. Die in den Studien mit Nuvaxovid beobachteten Nebenwirkungen seien in der Regel “leicht bis mittelschwer” gewesen, so die EMA weiter. Am häufigsten waren demnach Schmerzen an der Injektionsstelle, Müdigkeit, Muskelschmerzen, Kopfschmerzen, allgemeines Unwohlsein, Gelenkschmerzen und Übelkeit oder Erbrechen.
Wenn eine Person den Impfstoff erhält, erkennt ihr Immunsystem die Proteinpartikel als fremd und produziert natürliche Abwehrkräfte gegen sie. Im Gegensatz zu klassischen Totimpfstoffen enthält das Novavax-Mittel keine abgetöteten Viren. Die eigentliche Zulassung für die EU erfolgt durch die Europäische Kommission, was aber als reine Formalie gilt.
Foto: Europäische Arzneimittel-Agentur, über dts Nachrichtenagentur
Kontakt:
| Newsroom: | |
| Pressekontakt: | Deutsche Textservice Nachrichtenagentur GmbH Mansfelder Straße 56 06108 Halle (Saale) Deutschland |

- Dax startet schwächer – Meta-Ausblick drückt Stimmung - 25. April 2024
- Buschmann will mit Zehn-Punkte-Plan EU-Bürokratie reduzieren - 25. April 2024
- Spionageaffäre: Wadephul wirft AfD-Spitze Führungsschwäche vor - 25. April 2024