Die Bedeutung von Nachhaltigkeit, Klimaneutralität und umweltfreundlicher Mobilität nimmt kontinuierlich zu. Nicht umsonst streben viele Verbraucher eine nachhaltige Lebensweise an. Dank neuester Entwicklungen gibt es mittlerweile zahlreiche Möglichkeiten, um Wohnen, Ernährung und Mobilität umweltfreundlicher zu gestalten.
Eine Verkehrswende, die den Fokus auf Green Mobility legt, wird als entscheidender Schritt in Richtung Klimaneutralität angesehen. In dem Whitepaper „Fahrt aufnehmen in Richtung Verkehrswende: Eine Studie zum Thema Green Mobility und nachhaltige Fortbewegung“ von SIXT share werden die verschiedenen nachhaltigen Fortbewegungsmethoden eingehend untersucht. Die Studie bietet einen Einblick in die aktuelle öffentliche Meinung zu verschiedenen Fortbewegungsmitteln und verdeutlicht deren Bedeutung für die Zukunft der Mobilität.
Aufbau der Studie
Um Erkenntnisse über die Einstellungen und Gewohnheiten von 600 Personen in Bezug auf Umweltschutz und Green Mobility zu gewinnen, führte SIXT share, ein Anbieter von Autovermietungen und Carsharing-Diensten, eine Online-Umfrage durch. Die Teilnehmer der Umfrage waren zwischen 14 und 99 Jahre alt, um eine breite Altersstreuung sicherzustellen. Sie wurden in sieben Altersgruppen eingeteilt, darunter 14- bis 17-Jährige, 18- bis 24-Jährige, 25- bis 34-Jährige, 35- bis 44-Jährige, 45- bis 54-Jährige, 55- bis 64-Jährige und 65- bis 99-Jährige. Die Altersgruppe der 25- bis 34-Jährigen war dabei am häufigsten vertreten. Der Test wurde ausschließlich in den drei deutschen Großstädten Berlin, Hamburg und München durchgeführt, um eine repräsentative Stichprobe zu bekommen. Die Ergebnisse und Ansätze für umweltfreundliche Mobilität im Alltag sind in einem ausführlichen Whitepaper zusammengefasst.
Diese Rolle spielt der Umweltschutz
Die Umweltbelange stehen bei allen Befragten im Mittelpunkt ihres Denkens. Es herrscht allgemeine Übereinstimmung darüber, dass der Schutz der Umwelt von großer Bedeutung ist. Die Mehrheit der Befragten verfolgt einen nachhaltigen Lebensstil, indem sie Plastikvermeidung als Priorität betrachtet. Diese Maßnahme wird von mehr als der Hälfte der Teilnehmer hervorgehoben. Wenn es um umweltfreundliche Fortbewegungsmethoden geht, setzen über ein Drittel der Befragten auf das Fahrrad, was es auf den dritten Platz der am häufigsten genutzten Verkehrsmittel bringt. E-Scooter, E-Roller und Carsharing-Angebote sind ebenfalls beliebte Alternativen, die direkt danach folgen.
Vielfältige Gründe für Sharing-Angebote
Die Motivationen für die Nutzung von Sharing-Angeboten unterscheiden sich erheblich. Die oberste Priorität für die meisten Nutzer ist es, sicher nach Hause zu kommen, insbesondere nachts. In der Freizeit werden Sharing-Dienste oft genutzt, sei es für Treffen mit Freunden, spontane Spritztouren oder Wochenendausflüge. Dies trifft besonders auf E-Scooter zu, da mehr als die Hälfte der Befragten angab, sie aus reinem Vergnügen zu nutzen. Beim Carsharing stehen hingegen eher praktische Aspekte im Vordergrund: Viele nutzen die Dienste, um schwer erreichbare Ziele zu erreichen oder um schnell von einem Ort zum anderen zu gelangen. Darüber hinaus erweisen sich Carsharing-Angebote als äußerst nützlich für Transportaufgaben wie Umzüge oder größere Einkäufe.
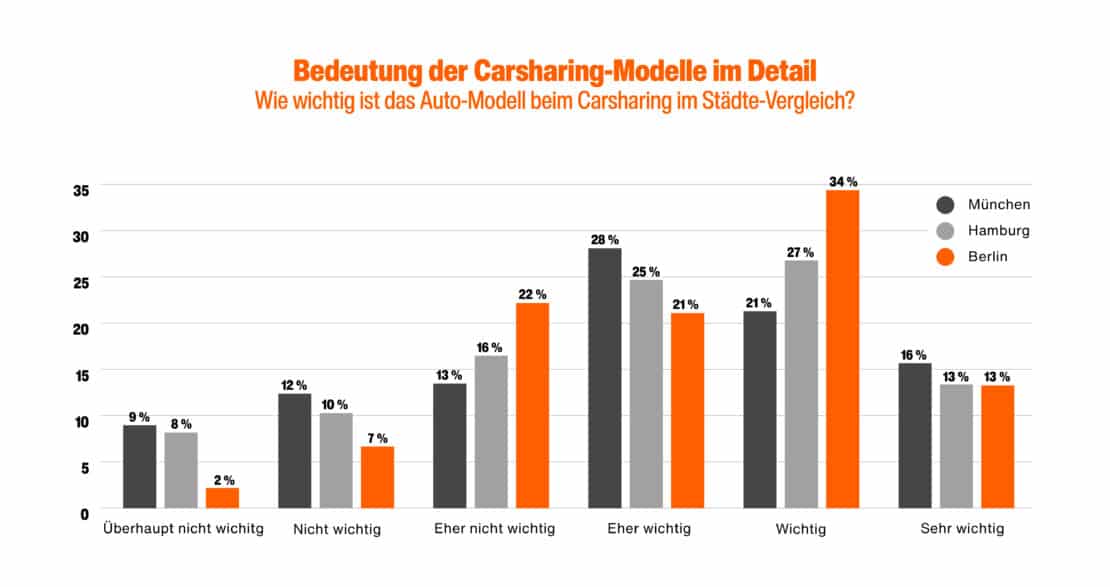
Die Bedeutung des Fahrzeugmodells beim Carsharing
Für mehr als die Hälfte der Befragten spielt das Fahrzeugmodell bei der Auswahl von Carsharing-Diensten eine entscheidende Rolle. Ein erhöhter Komfort und ein angenehmeres Fahrerlebnis sind die Hauptgründe dafür. Speziell die Möglichkeit, ein Fahrzeug auszuwählen, das den individuellen Bedürfnissen und Vorlieben entspricht, ist für viele Nutzer von großer Bedeutung. Dabei stehen Aspekte wie Raumangebot, Ausstattung und Fahrleistung für ein optimales Fahrerlebnis im Fokus.
Steigende Beliebtheit von Elektroautos
Elektroautos gewinnen zunehmend an Beliebtheit, was sich auch in der Umfrage widerspiegelt. Viele Teilnehmende, die bisher keine Erfahrung mit Elektroautos gemacht haben, zeigen großes Interesse daran, dies zu ändern. Primär jüngere und ältere Befragte würden die Gelegenheit nutzen, ein Elektroauto über Carsharing zu nutzen und bevorzugen es gegenüber einem Fahrzeug mit Verbrennungsmotor.
Bild: @ sixt.de
















